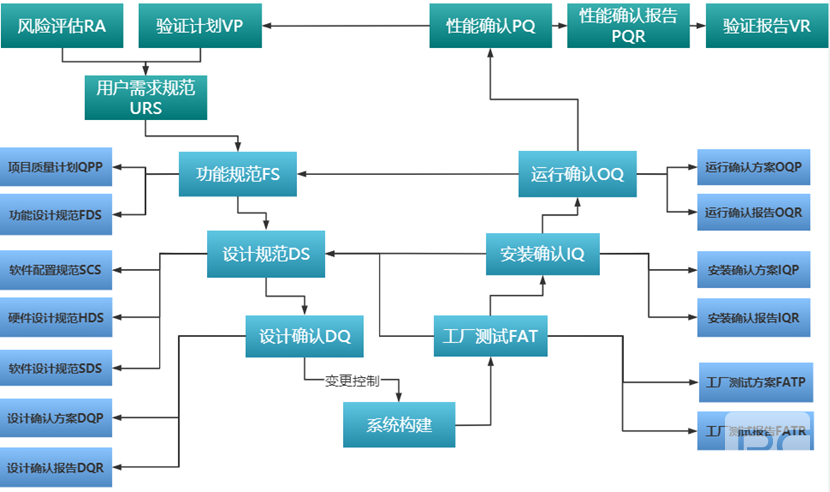
从 URS(用户需求规范) 出发,历经 FS/DS(功能/设计规范)、DQ/IQ/OQ/PQ(设计/安装/运行/性能确认) 等一系列严谨环节,最终生成 VR(验证报告)。每一步都关联着海量文档、严格测试与交叉确认。
这意味什么?
这意味着,选择一套电子批记录系统,您购买的不仅是一套软件,更是一个需要投入大量时间、人力和专业经验去完成的巨大验证工程。许多项目在此望而却步,或中途因系统“先天不足”而验证失败,导致投资沉没。
我们的解决方案:GMPEBR —— 为“验证通过”而生的EBR电子批记录系统
我们深刻理解,顺利、高效地通过CSV验证,是您项目成功的唯一标志。 因此,GMPEBR从设计之初,就内嵌了完整的验证支持体系,化“被动合规”为“主动赋能”。
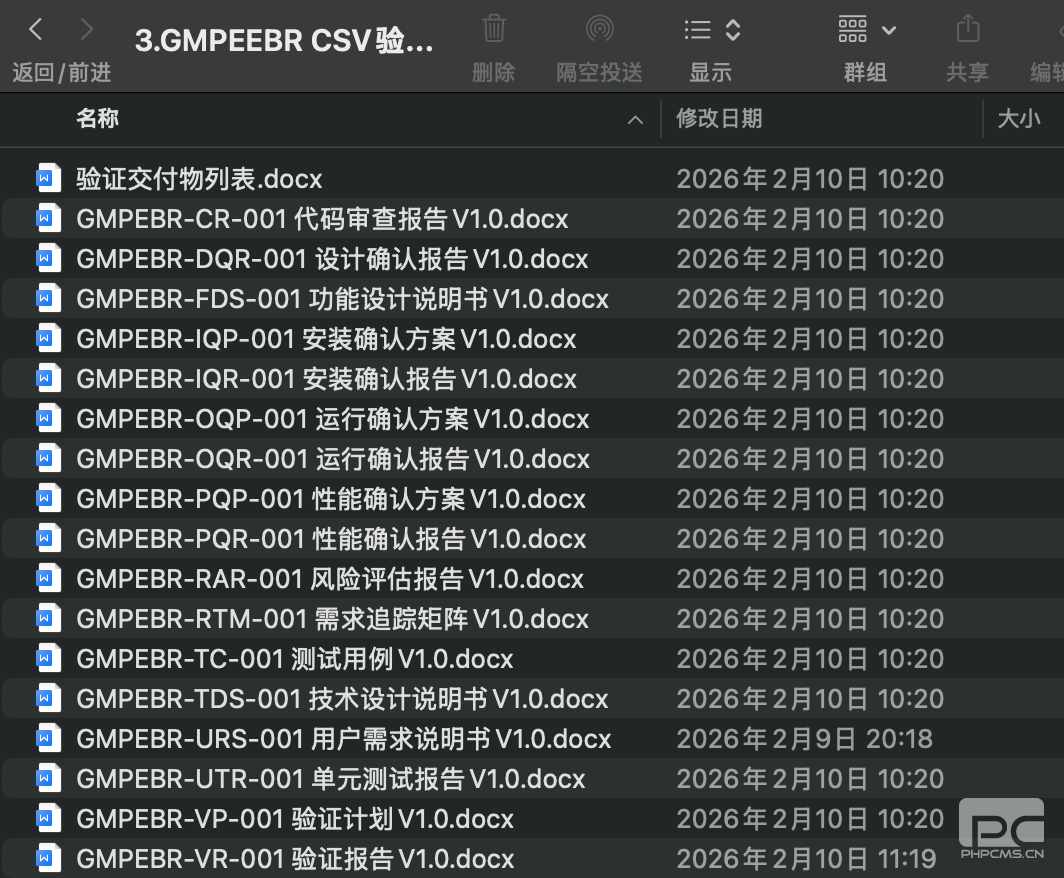
1. 提供完整的“验证就绪”交付包
您获得的不仅是一个系统,更是一套完整的验证支持体系,包括但不限于:
-
可配置的URS/FS/DS模板:基于行业最佳实践,帮助您快速、准确地定义需求与规范。
-
系统架构与设计说明:完全透明的系统设计文档,轻松应对 “设计确认(DQ)”。
-
开箱即用的测试用例库:预置大量符合GAMP 5要求的IQ/OQ/PQ测试脚本,极大缩短测试周期。
-
详尽的审计追踪与电子签名报告:内置符合21 CFR Part 11及欧盟附录11要求的功能证明,让“性能确认(PQ)” 水到渠成。
2. 配置化,而非定制化 —— 从根本上降低验证风险
GMPEBR采用成熟的行业模型,通过可视化配置而非底层代码开发,来适应您的流程。这意味着:
-
变更可控:任何调整都在受控的配置界面完成,变更影响清晰可溯,极大简化 “变更控制” 流程。
-
升级无忧:标准化的产品升级,不会破坏您已有的验证状态。
3. 我们不仅是供应商,更是您的验证合作伙伴
我们的团队由深谙GMP与计算机系统验证的专家组成,能为您提供:
-
从URS到VR的全程咨询:协助您梳理需求,制定验证主计划(VMP)。
-
联合执行支持:在IQ/OQ/PQ关键阶段,提供现场或远程支持,确保测试顺利进行。
-
交付完整的验证文件:协助您整理、生成最终提交给监管机构的 “验证报告(VR)”。
别再让复杂的验证流程,阻碍您拥抱生产效率与合规等级的飞跃。
GMPEBR,一套让验证从“绊脚石”变为“垫脚石”的电子批记录系统。