制药与医疗器械行业,质量体系文件的规范化管理不仅是企业日常运营的基石,更是应对严苛法规监管(如FDA 21 CFR Part 11、NMPA GMP/GSP)的生命线。面对海量的文件审批、频繁的版本更新与复杂的权限控制,传统的人工管理模式往往导致效率低下、合规风险高企以及数据追溯困难。
GMPDMS文控管理系统,深度融合行业最佳实践,为您提供一站式的数字化文件全生命周期管理解决方案,助您轻松跨越合规门槛,实现质量管理水平的跨越式提升。
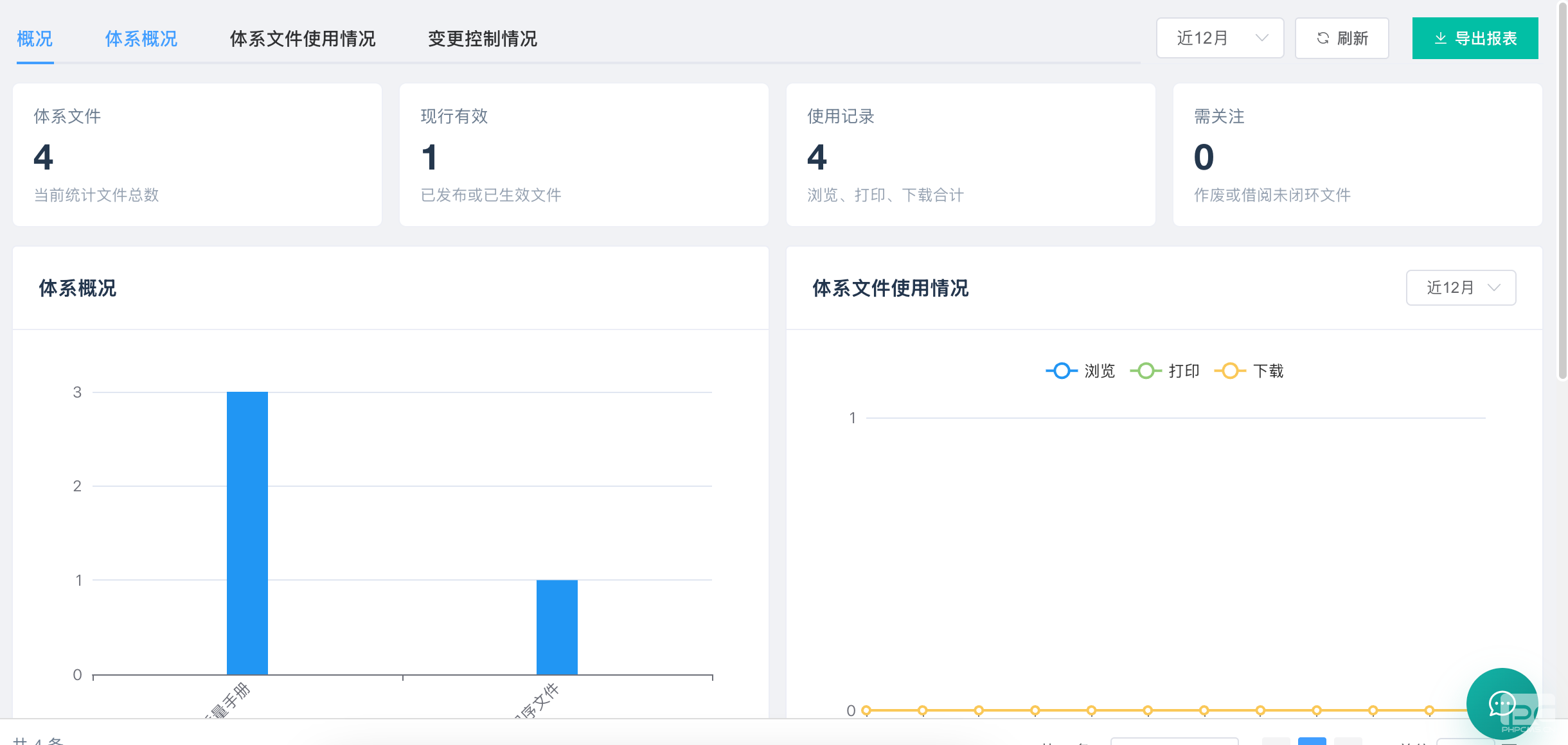
📊 驾驶舱级全局概览,业务动态一目了然
-
数据驱动决策:系统首页直观展示核心指标看板。从“体系文件总数”到“现行有效文件数”,从“高频使用记录”到“需关注的闭环文件”,所有关键信息尽收眼底。
-
多维度可视化分析:通过“体系概况”柱状图、“使用情况”折线图及“文件状态分布”环形图,管理者可实时洞察各部门(如工程设备部、生产制造部、质量保证部)的文件结构与流转效率,让管理更加精细化。
🛡️ 全链路合规管控,杜绝质量隐患
-
严谨的变更控制(ECR/ECO):系统内置严格的变更控制流程。图表化的“变更控制情况”追踪,精确记录每一次文件的新增、修订、变更与作废动作,确保“受控”状态下的每一次修改都有据可查,完美契合GMP对文件修订历史的严格审计要求。
-
闭环式状态流转:通过“文件状态分布”图,清晰区分已生效、已归档(archived)及已发布(published)的文件。配合顶部的“体系文件使用情况”与“变更控制情况”标签页,确保文件从起草、审核、批准到分发、作废的全链路闭环管理,杜绝非受控文件的流通。
🗄️ 精细化文件生命周期管理
-
多维统计与快速检索:在“多维度文件统计明细”中,每一份文件(质量手册、程序文件等)的编号、类型、归属目录及具体的操作记录(浏览/打印/下载次数、修订历史)均被详细记录。支持按名称、编号、目录等多条件模糊搜索,配合分页展示,海量文件也能精准定位。
-
深度定制化配置:左侧导航栏展示了系统强大的底层支撑能力。从“基础配置”到“流程中心”,管理员可根据企业组织架构和业务需求,灵活搭建审批流、配置权限矩阵,满足不同规模企业的个性化管理诉求。
🚀 核心应用场景:重塑文件管理价值
-
质量体系文件无纸化:告别繁琐的纸质审批流转,缩短文件生效周期,提升跨部门协作效率。
-
严格的权限与审计追踪:精确到个人的查看、打印、下载权限控制,结合系统自动留痕的审计追踪功能,完美应对国内外药监机构的现场核查。
-
培训与考核一体化:文件生效自动触发培训任务与考核流程,确保相关人员及时掌握最新质量要求。
-
供应商与外来文件管理:有效管理供应商提供的技术资料及国家/行业标准,防止过期文件误用。