在药品与医疗器械行业,每一次监管检查、每一次质量回溯,都是一次对质量体系运行效率和数据完整性的全面考验。传统模式下,企业往往需要耗费数日甚至数周,在浩如烟海的纸质或零散电子文件中,手工拼接出一批产品从物料到成品的“全生命周期故事”,过程繁琐且极易出错。而这一切,在GMPEBR电子批记录系统最新发布的“一键批记录追溯”功能下,被彻底重构。
今天,我们为您揭开这款革命性质量数字化平台的神秘面纱,看它如何将复杂的质量追溯,变成一次点击的瞬间穿透。
一、核心功能揭秘:不止于记录,更是全景质量关联
1. 全链穿透,一览无余
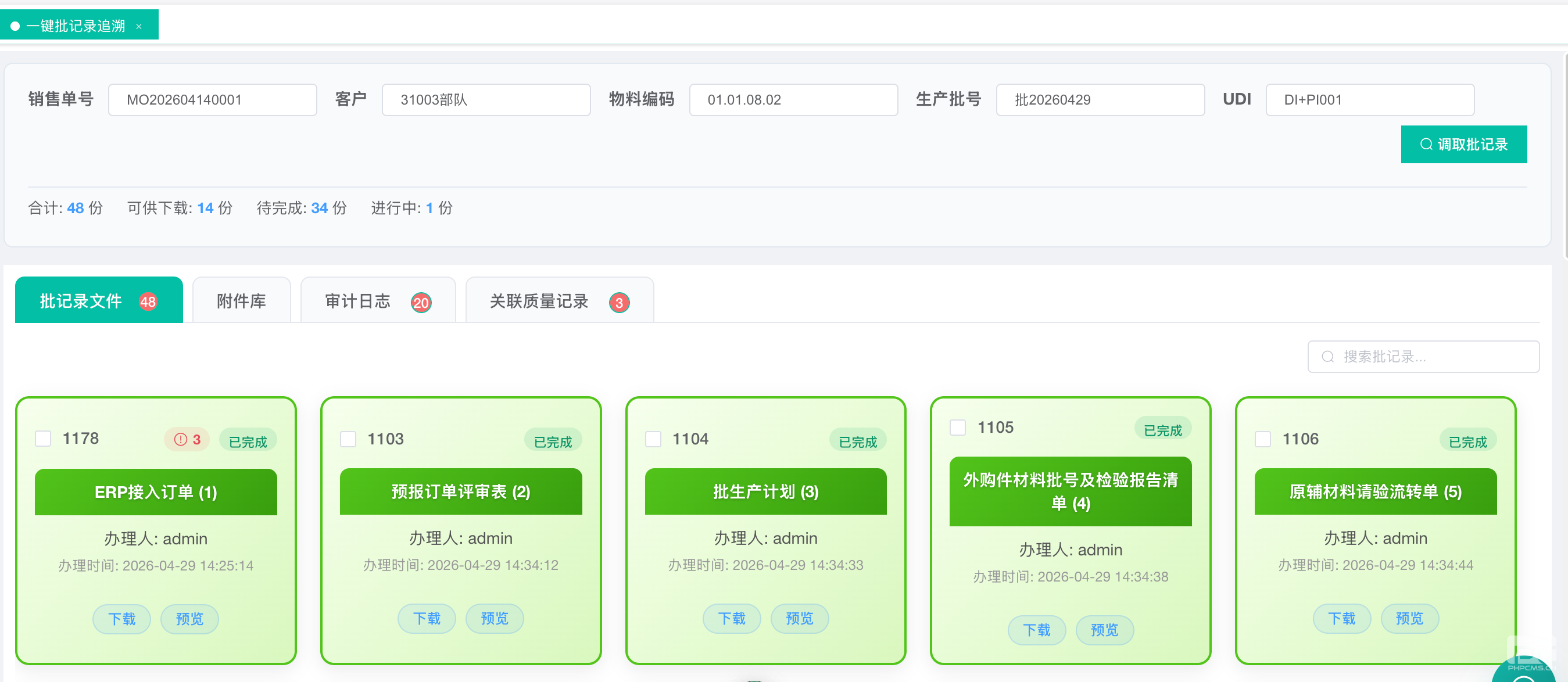
系统以唯一的生产批号为索引,一键即可调取与该批产品相关的全部数字足迹。如图所示,从ERP订单接入、生产计划、物料请验,到每一份检验报告,多达48份文件(已完成14份,流程中34份)的状态清晰可辨,支持一键预览与下载,彻底告别文件“躲猫猫”。

2. 超强关联,洞悉因果
这不仅是文件的聚合,更是质量逻辑的还原。系统核心突破在于,它能自动串联起批记录执行过程中触发的所有偏差、CAPA(纠正与预防措施)和变更流程。
-
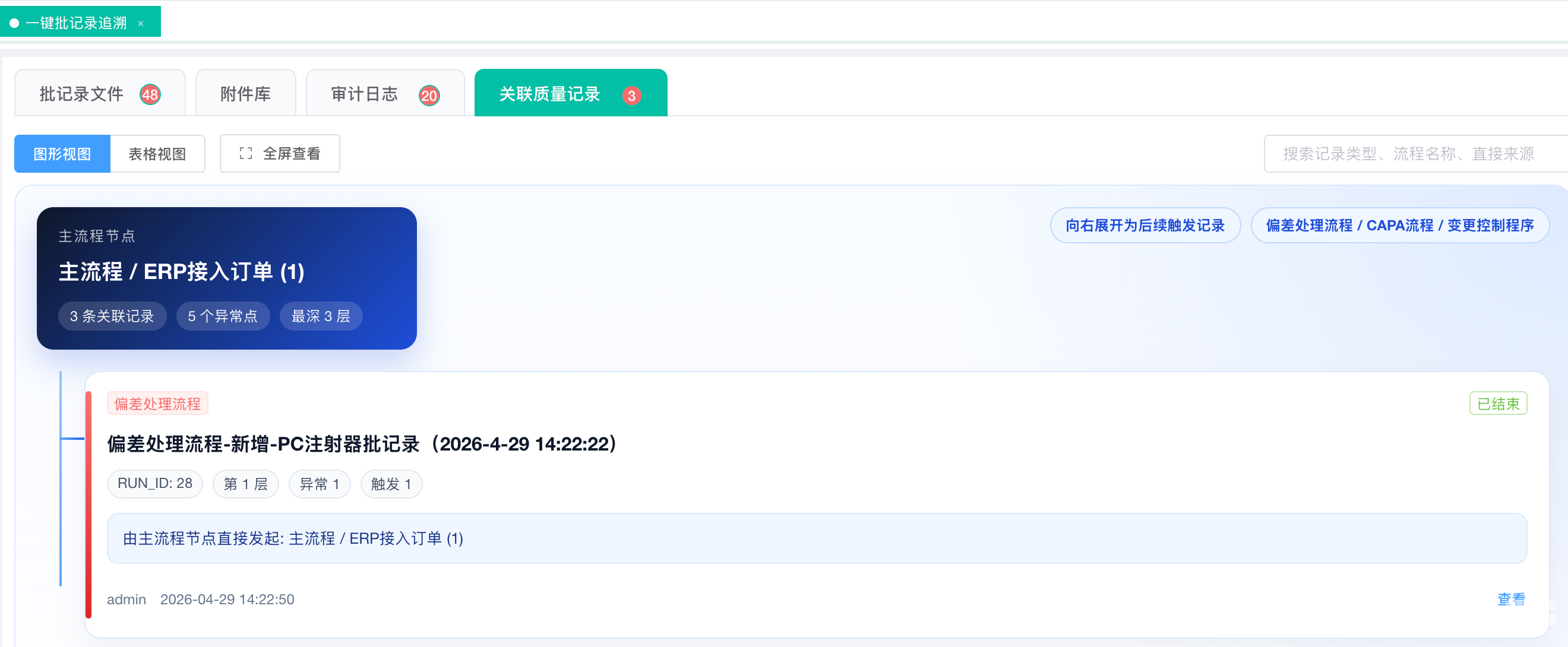
场景还原:当“ERP接入订单”环节触发一个“偏差处理流程”,系统不仅记录此事件,更能自动追踪由此偏差引发的后续“CAPA流程”,以及为根除问题而发起的“变更控制程序”。
-
可视化图谱:如上图所示,系统直观展示“主流程→偏差→CAPA→变更”的完整传导链与层级关系,让质量事件的“前世今生”一目了然,为根本原因分析提供无可辩驳的电子证据链。
3. 审计追踪,全程留痕
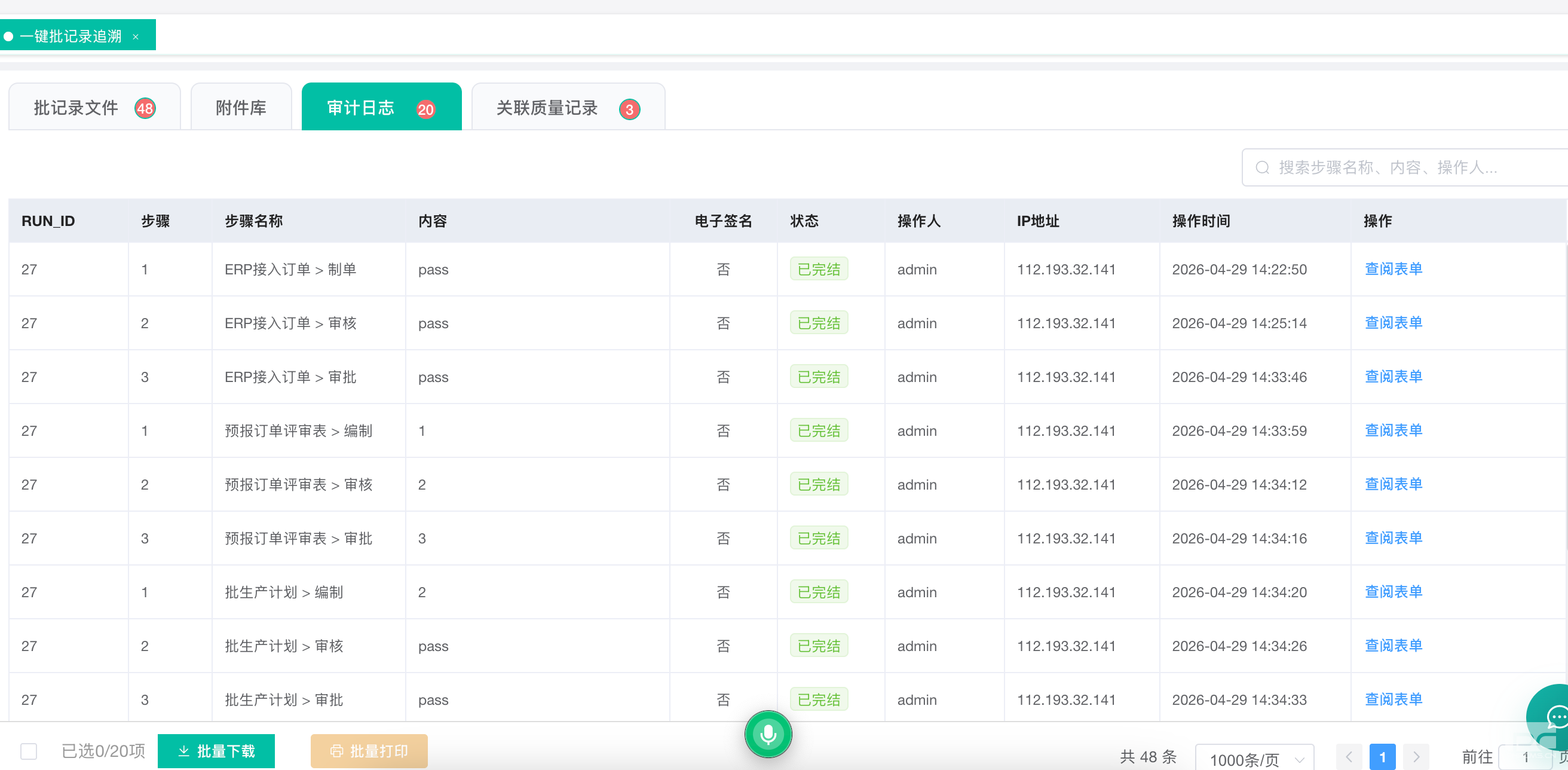
满足FDA 21 CFR Part 11及中国GMP附录最严苛要求。独立的“审计日志”标签页,记录每一次操作的人员、时间、IP地址、具体动作(如“审核pass”)及电子签名状态。所有对数据的创建、修改、审核行为均完整、不可篡改地留痕,确保数据完整性(ALCOA+原则)。
二、为医疗器械行业深度定制的合规引擎
4. 内置UDI全程记录
系统深度整合医疗器械唯一标识(UDI)要求,在追溯门户中直接展示产品DI+PI信息,确保从生产记录到上市标识的贯通,轻松应对中国及全球UDI法规的追溯要求。
5. 驱动高效的远程审计与电子放行
该功能极大赋能了“远程审计”和“委托生产电子放行”等新业态、新要求。委托方质量负责人可随时随地登录系统,一键穿透式审查受托方完整、关联的生产与质量记录,高效完成上市放行决策,显著降低合规成本与时间。
6. 实时数据采集,防错防呆
系统支持与生产设备、检测仪器、LIMS、ERP等深度集成,关键工艺参数、检验数据可自动采集、回填至批记录,杜绝人工转录错误。在追溯时,可随时调阅原始数据,验证生产过程受控状态。
三、客户价值:从“应对检查”到“质量赋能”
-
迎检效率提升90%以上:将以往数天准备的检查材料,压缩为“分钟级”响应。检查官可自主查看,质量人员无需疲于奔命地找文件。
-
质量风险实时掌控:管理者可实时洞察生产过程中的异常趋势及闭环效率,从“事后补救”转向“事前预防、事中控制”。
-
为数字化合规提供基石:该功能是满足《医疗器械生产质量管理规范(2025版)》、《药品记录与数据管理要求》等法规对数据关联性、可追溯性核心要求的最优解。
专家点评
“一个好的数字化质量系统,不仅要做‘记录仪’,更要做‘连接器’和‘放大镜’。”行业资深质量数字化专家评价道,“GMPEBR的‘一键追溯’功能,精准地抓住了从‘无纸化’迈向‘智能化’的关键——即打破数据孤岛,构建以产品批次为核心的质量全景图。这不仅是效率工具,更是质量决策和持续改进的战略资产。”
关于GMPEBR:GMPEBR是面向制药与医疗器械行业的一体化、闭环式数字化质量平台。以电子批记录(EBR)为核心,深度集成文档管理(DMS)、培训、偏差、变更、CAPA等全质量流程,致力于用领先的数字技术,助力生命科学企业构建坚实、高效、智能的质量管理体系,保障患者安全,驱动卓越运营。
欲体验“一键穿透”式质量追溯,欢迎联系我们获取演示 18180734225。